Resumen de servicios de cumplimiento con el MDR de la UE
El reglamento de productos sanitarios de la UE (MDR) entró en vigor el 26 de mayo de 2021, después de una transición de 3 años y un año más de prórroga por la pandemia de la COVID-19. Los productos que se lancen en el mercado de la UE ahora deben cumplir con estas normativas y deben tener el marcado CE según el MDR de la UE por los organismos notificados acreditados de acuerdo a estas normativas. Sin embargo, los productos que llevan el marcado CE de acuerdo con el MDR de la UE tienen períodos de gracia para cumplir completamente con los requisitos del MDR de la UE. Durante el período de gracia, los productos certificados por la MDD y el MDR de la UE coexistirán en el mercado con las mismas condiciones indiscriminadamente. Freyr brinda servicios de cumplimiento con el MDR de la UE sin parangón para ayudar a las empresas de productos sanitarios a cumplir con los requisitos del MDR de la UE oportunamente.
Agende una reunión con los expertos en MDR de la UE
La transición del MDR y la clasificación de nuevos productos
El reglamento de productos sanitarios europeo (MDR) será efectivo en todos los estados miembros de la UE y en los estados de la Asociación Europea de Libre Comercio (AELC) desde mayo de 2021 y le brinda a los fabricantes un período de transición de 4 años para completar la certificación MDR de la UE.
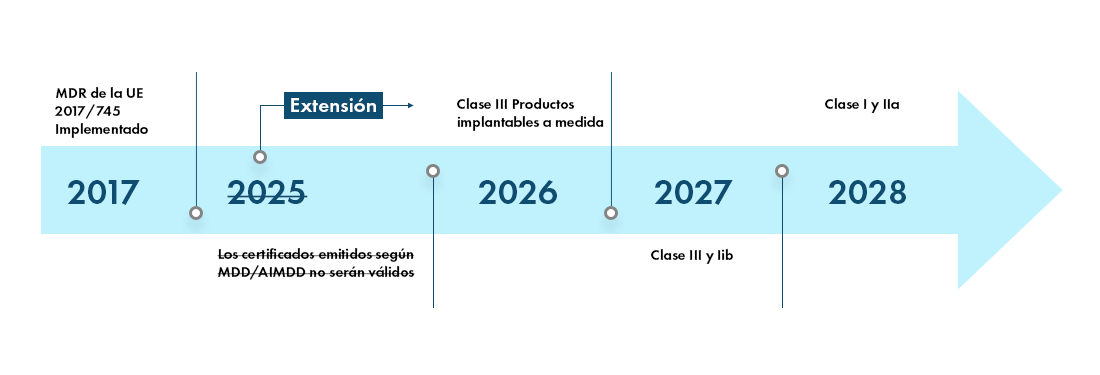
El nuevo reglamento de productos sanitarios europeo (MDR) ha introducido cambios en el sistema de clasificación de productos existentes. Por ejemplo:

Desde la identificación de los cambios exactos que se deben hacer hasta implementarlos en tiempo real, los fabricantes pueden enfrentar diversos desafíos para cumplir con los requisitos del MDR de la UE. Desde decodificar una nueva estructura, clasificar un producto correctamente hasta reunir y enviar toda la información, se requerirá un método reglamentario más detallado y multidisciplinario para los fabricantes para manejar el nuevo reglamento de productos sanitarios europeos. Aplicando un análisis de brecha estricto, Freyr ayuda a sus clientes con el estado actual y brinda la acción reglamentaria pertinente para la transición y el cumplimiento con el MDR de la UE.
LA EXPERIENCIA DE FREYR
- Desarrollo de una estrategia clara para implementar el reglamento de productos sanitarios.
- Conocimiento de la legislación nueva, realización de análisis de brecha sobre los sistemas de gestión de calidad (SGC) actuales y los procesos establecidos.
- Desarrollo de un plan detallado con un método multidisciplinario para determinar los aspectos del sistema de calidad que requerirán modificaciones en siguiendo el nuevo reglamento de productos sanitarios de la UE.
- Conformación de distintos equipos para analizar el alcance, la clasificación, el manejo de los SGC de los productos, etc., dentro de la organización con un único punto de contacto en cada equipo.
- Distribución y planificación de los recursos.
- Evaluación de la interacción de los SGC con otros reglamentos y uso de esta oportunidad para optimizar procesos mientras se flexibiliza la incorporación de cambios a futuro.
- Análisis de la información de evaluación establecida para cualquier requisito adicional que defina el MDR.
- Coordinación de las expectativas y el plan de transición con los organismos notificados de la UE.
- Análisis de brecha para los productos sanitarios existentes de la normativa MDD al MDR de la UE.
- Ayuda de principio a fin para desarrollar un informe de evaluación clínica (CER), incluyendo la búsqueda de bibliografía sobre lineamientos del reglamento de productos sanitarios europeo (MDR de la UE).
- Servicios de principio a fin para los informes de seguimiento de poscomercialización (PMSR), el informe periódico de seguridad actualizado (PSUR) y el informe de seguridad y rendimiento clínico (SSCP).
- Aumento de los recursos reglamentarios con opciones de despliegue en el país como en el extranjero.
- Servicios de representante autorizado europeo (EAR).
- Ayuda en el cumplimiento y presentación de MDR a los organismos notificados.
- Inteligencia reglamentaria que cubre el servicio de importación de distintos mercados regulados.
- Auditorías simuladas de cumplimiento de los SGC.
- Sistema de gestión de documentos y herramientas para empresas del MDR.
- Clasificación y reclasificación de los productos según el riesgo.
- Implementación y consultoría del sistema de identificación única.
- Servicios de cumplimiento con el seguimiento de poscomercialización del reglamento de productos sanitarios de la UE.
- Consultoría sobre gestión de riesgos ISO 14971.
- Capacitaciones internas y a distancia.
- Personas responsables de los servicios de ayuda y del cumplimiento de la normativa.
- Identificación de los organismos notificados del MDR.
Para obtener ayuda de principio a fin sobre el MDR de la UE, contáctese con Freyr.